СОСТАВ И ФОРМА ВЫПУСКА:
Таблетки, покрытые пленочной оболочкой.
1 таблетка содержит 150 мг или 500 мг капецитабина; дополнительные компоненты: лактоза, натрия кроскармеллоза, гипромеллоза, целлюлоза микрокристаллическая, магния стеарат
Оболочка:
для 150 мг – Opadry Pink 03A84408 (гипромеллоза, титана диоксид (Е 171), железа оксид желтый (Е172), железа оксид красный (Е172), тальк)
для 500 мг – Opadry Pink 03A84598 (гипромеллоза, титана диоксид (Е 171), железа оксид желтый (Е172), железа оксид красный (Е172), тальк).
Упаковка:
По 10 таблеток в блистере, по 1 или 6, или по 12 блистеров в картонной коробке.
ФАРМАКОЛОГИЧЕСКИЕ СВОЙСТВА:
Фармакодинамика. Капецитабин – производное фторпиримидина карбамата, пероральный цитостатик, который активируется в ткани опухоли и оказывает на нее селективное цитотоксическое действие. Сам капецитабин не оказывает цитотоксического действия, однако превращается в цитотоксическое соединение – фторурацил (5-ФУ). Образование 5-ФУ происходит в ткани опухоли под действием опухолевого ангиогенного фактора тимидинфосфорилазы, что, таким образом, сводит к минимуму системное воздействие 5-ФУ на здоровые ткани организма.
Последовательная ферментная биотрансформация капецитабина в 5-ФУ создает в клетках опухоли более высокие его концентрации, чем в окружающих здоровых тканях. После приема капецитабина больным раком толстой кишки концентрация 5-ФУ в ткани опухоли выше, чем в здоровых тканях, в 3,2 раза. Отношение концентраций 5-ФУ в ткани опухоли и плазме – 21,4, отношение его концентрации в здоровых тканях и в плазме – 8,9. Активность тимидинфосфорилазы в первичной колоректальной опухоли в 4 раза выше, чем в окружающих здоровых тканях.
В опухолевых клетках у больных раком молочной железы, желудка, толстой кишки, шейки матки и яичников содержится больше тимидинфосфорилазы, которая способна превращать 5'-ДФУР (5'-дезокси-5-фторуридин) в 5-ФУ, чем в соответствующих здоровых тканях .
Как здоровые, так и опухолевые клетки метаболизируют 5-ФУ в 5-фтор-2-дезоксиуридина монофосфат (ФдУМФ) и 5-фторуридин трифосфат (ФУТФ). Эти метаболиты повреждают клетки путем двух различных механизмов. Во-первых, ФдУМФ и фолатный кофактор N5 “10-метилентетрагидрофолат связываются с тимидилатсинтазой (ТС) с образованием ковалентно связанного третичного комплекса. Эта связь подавляет образование тимидилата из урацила. Тимидилат является предшественником тимидина трифосфата, который, в свою очередь, очень важен для синтеза ДНК, так как недостаточность этого вещества может привести к угнетению клеточного деления. Во-вторых, в процессе синтеза РНК транскрипционные ферменты ядра могут ошибочно включить в нее ФУТФ вместо уридина трифосфата (УТФ). Эта метаболическая ошибка нарушает процессинг РНК и синтез белка.
Фармакокинетика.
Всасывание. После приема капецитабин быстро и полностью всасывается, после чего проходит его биотрансформация в метаболиты 5'-дезокси-5-фторцитидин (5'-ДФЦТ) и 5'-ДФУР. Прием пищи уменьшает скорость всасывания капецитабина, однако не оказывает значительного влияния на величину площади под кривой «концентрация-время» (AUC) 5'-ДФУР и последующего метаболита 5-ФУ. При назначении препарата в дозе 1250 мг/м2 после приема пищи на 14-й день максимальные концентрации Сmax капецитабина, 5'-ДФЦР, 5'-ДФУР, 5-ФУ и ФБАЛ составляли соответственно 4,47, 3,05, 12, 1, 0,95 и 5,46 мкг/мл. Время достижения максимальной концентрации Т max равна 1,50, 2,00, 2,00, 2,00 и 3,34 ч, a AUC – 7,75, 7,24, 24,6, 2,03 и 36,3 мкг х ч/мл соответственно.
Связь с белками. Для капецитабина, 5'-ДФЦТ, 5'-ДФУР и 5-ФУ связь с белками (главным образом с альбумином) составляет соответственно 54%, 10%, 62% и 10%.
Метаболизм. Метаболизируется в печени под действием карбоксилэстеразы к метаболита 5'-ДФЦТ, который затем трансформируется в 5'-ДФУР под действием цитидиндезаминазы, что находится в основном в печени и опухолевых тканях. Концентрации 5-ФУ и его активных фосфорилированных анаболитив в опухоли значительно превышают уровни в здоровых тканях, за счет чего обеспечивается относительная селективность цитотоксического эффекта. AUC для 5-ФУ в 6-22 раза меньше, чем после струйного введения 5-ФУ в дозе 600 мг / м 2 метаболитов капецитабина становятся цитотоксическими только после преобразования в 5-ФУ и анаболиты 5-ФУ.
Затем 5-ФУ катаболизируется с образованием неактивных метаболитов – дигидро-5-фторурацила (ФУН2), 5-фторуреидопропионовои кислоты (ФУПК) и а-фтор (3-аланина (ФБАЛ) этот процесс проходит под влиянием дигидропиримидиндегидрогеназы (ДПД), активность которой ограничивает скорость реакции.
Вывод. Период полувыведения (Т 1/2 ) капецитабина, 5'-ДФЦР, 5'-ДФУР, 5-ФУ и ФБАЛ составляет соответственно 0,85, 1,11, 0,66, 0,76 и 3,23 часа. Фармакокинетика капецитабина изучалась для диапазона доз 502-3514 мг / м2 / день. Фармакокинетические параметры капецитабина, 5'-ДФЦТ и 5'-ДФУР на 1-й и 14-й день одинаковы. AUC 5-ФУ увеличивается до 14-го дня на 30-35% и больше не повышается (22-й день). В диапазоне терапевтических доз фармакокинетические параметры капецитабина и его метаболитов, за исключением 5-ФУ, имеют дозозависимый характер.
После приема метаболиты капецитабина в основном выводятся с мочой. Экскреция с мочой – 95,5%, с калом – 2,6%. Основным метаболитом в моче является ФБАЛ, который составляет 57% от принятой дозы. Примерно 3% принятой дозы выводится с мочой в неизмененном виде.
Комбинированная терапия.
В ходе исследований фармакокинетики не было обнаружено влияния Капецитабина на фармакокинетику доцетаксела и паклитаксела (Cmax и AUC) и влияния доцетаксела и паклитаксела на фармакокинетику Капецитабина и 5'-ДФУР (наиболее важного метаболита капецитабина).
Фармакокинетика в особых клинических группах.
Пол, наличие или отсутствие метастазов в печень до начала лечения, индекс общего состояния пациента, концентрация общего билирубина, сывороточного альбумина, активность АЛТ и ACT у больных раком толстой кишки не имели существенного влияния на фармакокинетику 5Г-ДФУР, 5-ФУ и ФБАЛ.
Больные с метастатическим поражением печени. У больных с легкой и умеренной степенью нарушения функции печени, обусловленным метастазами, клинически значимых изменений фармакокинетики капецитабина не наблюдается. Данные по фармакокинетике у больных с тяжелым нарушением функции печени отсутствуют.
Больные с нарушением функции почек . При разной степени (от легкой до тяжелой) почечной недостаточности фармакокинетика неизмененного препарата и 5-ФУ не зависящие от клиренса креатинина (КК). УК влияет на величину AUC 5'-ДФУР (увеличение AUC на 35% – при снижении КК на 50%) и ФБАЛ (увеличение AUC на 114% при снижении КК на 50%). ФБАЛ – метаболит, не имеет антипролиферативное активности; 5'-ДФУР – непосредственный предшественник 5-ФУ.
Пожилой возраст. Возраст не влияет на фармакокинетику 5'-ДФУР и 5-ФУ. AUC ФБАЛ увеличивается у больных в возрасте от 65 лет (увеличение возраста на 20% сопровождалось увеличением AUC ФБАЛ на 15%), что, вероятно, обусловлено изменением функции почек.
ПОКАЗАНИЯ:
Рак молочной железы:
- местный распространенный или метастатический рак молочной железы, в сочетании с доцетакселом после неэффективной химиотерапии, включающей препараты антрациклинового ряда.
- местный распространенный или метастатический рак молочной железы после неэффективной химиотерапии, включающей таксаны и препараты антрациклинового ряда, или при наличии противопоказания к терапии антрациклинами.
Рак ободочной кишки, колоректальный рак:
- рак ободочной кишки, в адъювантной терапии.
- препарат первого ряда для лечения колоректального рака с метастазами.
Рак пищевода и желудка:
- препарат первого ряда для лечения распространенного рака пищевода и желудка.
ПРИМЕНЕНИЕ:
Стандартная дозировка.
Препарат принимают внутрь, не позднее чем через 30 минут после еды, запивая водой.
Монотерапия.
Рак ободочной кишки, колоректальный рак и рак молочной железы рекомендуемая суточная доза Капецитабина составляет 2500 мг/м2 поверхности тела и применяется в виде трехнедельных циклов: принимают ежедневно в течение 2 недель, после чего делают недельный перерыв. Суммарную суточную дозу делят на два приема (по 1250 мг/м2 поверхности тела утром и вечером).
Комбинированная терапия.
Рак молочной железы по 1250 мг/м2 2 раза в сутки в течение 2 недель с последующей недельным перерывом в комбинациии с доцетакселом (75 мг/м 2 1 раз в 3 недели). Премедикация проводится перед введением доцетаксела в соответствии с инструкцией для применения доцетаксела.
Рак ободочной кишки, колоректальный рак, рак желудка и пищевода в режиме комбинированного лечения начальную дозу препарата необходимо уменьшить до 800-1000 мг / м2 2 раза в сутки в течение 2 недель с последующим недельным перерывом или до 625 мг / м 2 2 раза в сутки при непрерывном применении. Включение биологического препарата в схему комбинированного применения не повлияло на начальную дозу препарата. Общая рекомендуемая продолжительность адъювантной терапии у пациентов с раком ободочной кишки III стадии составляет 6 месяцев.
Противорвотные средства и премедикацию для обеспечения адекватной гидратации назначают пациентам, которые получают препарат в комбинации с цисплатином или оксалиплатином перед введением цисплатина в соответствии с инструкцией к применению цисплатина и оксалиплатина.
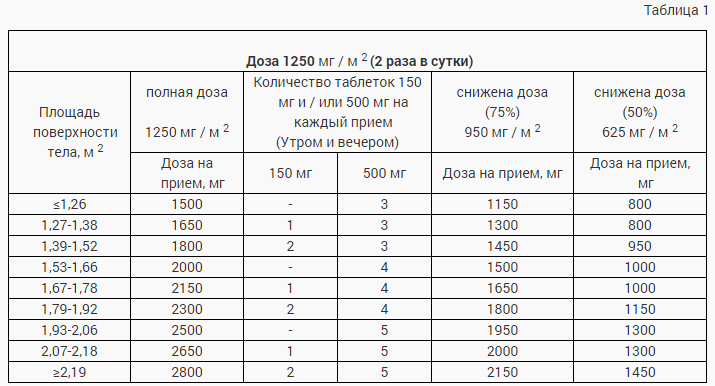
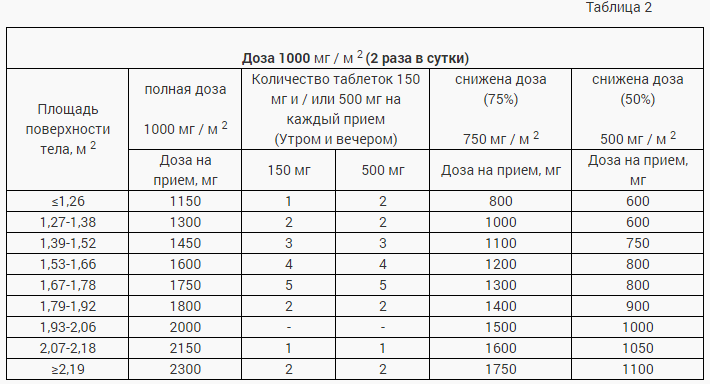
Дозу рассчитывают по площади поверхности тела. В таблицах 1, 2 приведены расчеты стандартной и пониженной доз (см. «Коррекция дозы в процессе лечения») для начальной дозы 1250 мг / м 2 или 1000 мг / м 2 .
Коррекция дозы в процессе лечения.
Общие рекомендации.
Явления токсичности при лечении Капецитабином можно устранить симптоматической терапией или изменением дозы препарата (прервав лечение или уменьшив дозу препарата). Если дозу пришлось уменьшить, в дальнейшем ее не увеличивают.
При явлениях токсичности, которые, по мнению врача, маловероятно станут серьезными будут угрожать жизни, применение препарата можно продолжать в той же дозе, не прерывая лечения и не сбавляя дозу препарата.
При токсичности I степени корректировать дозу не нужно. При токсичности II или III степени прием Капецитабина следует прекратить до исчезновения токсичности или уменьшению симптоматики до I степени. Прием Капецитабина можно возобновить в полной дозе или с коррекцией. При развитии признаков токсичности IV степени лечение следует прекратить до уменьшения симптоматики (до I степени), после чего применение препарата возобновляют в дозе, составляющей 50% от первоначальной. Пациентов, проходящих лечение Капецитабином, необходимо предупредить, что лечение нужно прекратить в случае развития умеренных или тяжелых токсических реакций. Если из-за токсичных явлений было пропущено несколько приемов капецитабина, то пропущенные дозы не требуется применять дополнительно, а просто продолжать запланированные циклы терапии.
Гематологическая токсичность.
Больным с исходным уровнем нейтрофилов <1,5х109/л и/или тромбоцитов <100х109/л нельзя назначать терапию капецитабином. Терапию следует приостановить при возникновении гематологической токсичности III и IV степени тяжести.
Общая комбинированная терапия.
В начале курса лечения при необходимости отсрочки терапии Капецитабином или иным лекарственным средством следует отсрочить также назначение других препаратов к периоду возможности назначения всех компонентов схемы.
При возникновении токсических явлений во время лечения, которые, по мнению врача, не связанные с применением капецитабина, терапию Капецитабином необходимо продолжать и провести коррекцию дозы других лекарственных средств-компонентов схемы в соответствии с инструкциями по применению.
В случае необходимости отмены других лекарственных средств-компонентов схемы лечения Капецитабином можно продолжить при достижении необходимых условий для повторного назначения препарата
Указанные рекомендации касаются всех показаний для применения и всех групп пациентов.
Коррекция дозы в особых случаях
Больные с нарушением функции печени, обусловленным метастазами
Для больных с метастазами в печени и легким или умеренным нарушением функции печени изменять начальную дозу не нужно. Однако таких пациентов нужно тщательно наблюдать. У пациентов с тяжелым нарушением функции печени препарат не изучался.
Больные с нарушением функции почек
Для больных с исходной умеренной почечной недостаточностью (клиренс креатинина 30-50 мл / мин) рекомендуется уменьшить начальную дозу до 75% от стандартной (1250 мг/м2). Пациентам с почечной недостаточностью легкой степени (клиренс креатинина 51-80 мл / мин) коррекция дозы не требуется.
При возникновении побочных явлений II, III или IV степени рекомендуется тщательный мониторинг и немедленная отмена лечения или изменение дозы. При снижении уровня креатинина менее 30 мл/мин лечение Капецитабином необходимо прекратить. Рекомендации по коррекции дозы при умеренной почечной недостаточности одинаковы как при монотерапии капецитабином, так и при комбинированной терапии. Рекомендации по расчету дозы приведены в таблицах 1 и 2.
Больные пожилого возраста
Корректировка начальной дозы при монотерапии капецитабином не нужно. Однако у больных старше 80 лет явления III и IV степеней токсичности развивались чаще, чем у молодых пациентов.
Рекомендуется тщательный мониторинг состояния больных пожилого возраста. При применении Капецитабина в комбинации с другими лекарственными средствами у больных пожилого возраста (≥ 65 лет) отмечалась большая частота нежелательных эффектов III и IV степеней токсичности, которые привели к отмене лечения, по сравнению с таковой у больных молодого возраста.
При лечении Капецитабином в комбинации с доцетакселом у больных старше 60 лет отмечалось увеличение частоты нежелательных эффектов III и IV степеней токсичности. Пациентам этой возрастной категории при комбинированном лечении Капецитабином и доцетакселом рекомендуется уменьшить начальную дозу Капецитабина до 75% (950 мг / м 2 раза в сутки). Расчеты приведены в таблице 2.
При лечении Капецитабином в комбинации с иринотеканом больным в возрасте до65 лет рекомендуется уменьшить начальную дозу Капецитабина до 800 мг/ м2 раза в сутки.
Дети.
Безопасность и эффективность препарата для детей не изучались.
ПРОТИВОПОКАЗАНИЯ:
Тяжелые, в том числе неожиданные, реакции на лечение фторпиримидинами. Гиперчувствительность к капецитабина или к любому компоненту препарата, или к фторурацила. Известный дефицит дигидропиримидиндегидрогеназы. Тяжелая лейкопения, нейтропения, тромбоцитопения. Тяжелые нарушения функции печени. Тяжелая почечная недостаточность (клиренс креатинина <30 мл / мин). Одновременный прием соривудином или его структурных аналогов типа бривудина.
ПОБОЧНЫЕ ЭФФЕКТЫ:
Общий профиль безопасности капецитабина базируется на основе данных более 3000 пациентов, получавших лечение препаратом в режиме монотерапии или в комбинации с различными схемами химиотерапии для различных показаний для применения. Профиль безопасности монотерапии препарата при метастатическом раке молочной железы, метастатическом колоректальном раке и раке ободочной кишки в адъювантной терапии является сопоставимым.
Наиболее частыми и/или клинически значимыми побочными реакциями, связанными с лечением, были реакции со стороны желудочно-кишечного тракта (диарея, тошнота, рвота, боль в животе, стоматит), ладонно-подошвенный синдром (ладонно-подошвенная эритродизестезия), слабость , астения, анорексия, кардиотоксическое, прогрессирование нарушения функции почек у пациентов с почечной недостаточностью, тромбоз/эмболия.
ОСОБЫЕ УКАЗАНИЯ:
Терапию капецитабином проводят под пристальным контролем врача. Нельзя проводить лечение препаратом в комбинации с другим лекарственным средством, если такое противопоказан.
Токсическое действие, зависит от дозы : диарея, боль в животе, тошнота, стоматит, ладонно-подошвенный синдром (синонимы – ладонно-подошвенная эритродизестезия или периферическая эритема, вызванная химиотерапией). Большинство нежелательных эффектов обратимы и не требуют полной отмены препарата, хотя может возникнуть необходимость в коррекции дозы или временной отмене препарата.
Диарея . Капецитабин может вызвать диарею, иногда тяжелую. Больных с тяжелой диареей следует тщательно наблюдать, проводя им регидратацию и восстановление потери электролитов при дегидратации. По показаниям как можно раньше рекомендуется назначать стандартные противодиарейные препараты (например, лоперамид). Диарея II степени по критериям Национального онкологического института Канады (NCIC СТС, версия 2) определяется как увеличение количества дефекаций до 4-6 раз в сутки или дефекации ночью, диарея III степени – как увеличение количества дефекаций до 7-9 раз в сутки или недержание кала и мальабсорбция. Диарея IV степени определяется как увеличение количества дефекаций ≥ 10 / сутки или массивная диарея с примесью крови, или необходимость назначения парентеральных вливаний. При необходимости дозу препарата следует уменьшить (см. Раздел «Способ применения и дозы»).
Дегидратация. Необходимо предупреждать развитие дегидратации и осуществлять коррекцию дегидратации в случае ее возникновения. Дегидратация может быстро развиться у больных с анорексией, астенией, тошнотой, рвотой или диареей. При появлении дегидратации II степени (или выше) лечения необходимо немедленно прекратить и провести коррекцию дегидратации. Восстановление лечение возможно при адекватной коррекции дегидратации. Коррекция дозы в случае возникновения преципитирующих побочных явлений проводится по мере необходимости.
Ладонно-подошвенный синдром (синонимы – ладонно-подошвенная эритродизестезия или периферическая эритема, вызванная химиотерапией). Проявлением кожной токсичности является развитие ладонно-подошвенного синдрома I-III ступеней токсичности. Время до появления синдрома при монотерапии составляет от 11 до 360 дней, в среднем – 79 дней.
Ладонно-подошвенный синдром I степени не затрагивает ежедневной активности больного и проявляется онемением, парестезиями, дизестезиями, покалыванием или покраснением ладоней и / или подошв, дискомфортом.
Ладонно-подошвенный синдром II степени проявляется болезненным покраснением и отеками кисти рук и / или подошв, вызванный этими проявлениями дискомфорт нарушает ежедневную активность больного. Ладонно-подошвенный синдром III степени определяется как влажная десквамация, образование язв, появление пузырей и острая боль ладоней и / или подошв и / или тяжелый дискомфорт, который не дает возможности пациентам передвигаться.
В случае появления ладонно-подошвенного синдрома II или III степени прием капецитабина следует прекратить до исчезновения симптомов или их уменьшения до I степени; при следующем появлении синдрома III степени дозу капецитабина нужно уменьшить (см. раздел «Способ применения и дозы»). Больным, которые одновременно получают Капецитабин и цисплатин, применение витамина B 6(пиридоксин) с целью симптоматического или вторичного профилактического лечения ладонно-подошвенного синдрома не рекомендуется, поскольку это может привести к снижению эффективности цисплатина.
Кардиотоксичность. Спектр кардиотоксичности при лечении капецитабином аналогичен таковому при применении других фторпиримидинов и включает инфаркт миокарда, стенокардию, аритмии, кардиогенный шок, внезапную смерть, остановку сердца, сердечную недостаточность и изменения ЭКГ. Эти побочные эффекты чаще характерны для больных ишемической болезнью сердца. При применении препарата сообщалось о случаях сердечных аритмий, стенокардии, инфаркта миокарда, сердечной недостаточности, кардиомиопатии. При назначении Капецитабина пациентам с клинически значимым заболеванием сердца, аритмиями и стенокардией необходимо проявлять осторожность.
Гипо- или гиперкальциемия . Во время лечения сообщалось о гипо- или гиперкальциемии.
Заболевания центральной или периферической нервной системы . При назначении Капецитабина пациентам с заболеванием центральной или периферической нервной системы, например метастазами в головной мозг или нейропатией, необходимо проявлять осторожность.
Сахарный диабет или нарушение уровня электролитов. При назначении Капецитабина пациентам с сахарным диабетом или нарушением уровня электролитов необходимо проявлять осторожность, поскольку применение капецитабина может приводить к ухудшению их состояния.
Антикоагулянты – производные кумарина . В ходе исследования взаимодействия наблюдалось существенное увеличение средней величины площади под кривой «концентрация-время» (AUC) S-варфарина (на 57%), что свидетельствует о наличии взаимодействия, вероятно, в результате угнетения капецитабином цитохрома Р450 2С9 фермента. Больным, которые одновременно принимают капецитабин и пероральные антикоагулянты – производные кумарина, необходимо проводить детальный мониторинг показателей свертывания крови (международное нормализованное отношение или протромбиновое время) и подбирать дозу антикоагулянта.
Нарушение функции печени. В связи с отсутствием данных о безопасности и эффективности для больных с нарушением функции печени необходимо тщательно мониторить применения препарата пациентам с нарушением функции печени легкой и средней степени тяжести независимо от наличия или отсутствия метастазов в печень. Если в результате лечения капецитабином наблюдается гипербилирубинемия, что превышает верхнюю границу нормы более чем в 3 раза, или повышается активность печеночных аминотрансфераз (АЛТ, ACT) больше чем в 2,5 раза по сравнению с верхней границей нормы, применение капецитабина следует прекратить. Лечение капецитабином можно восстановить при снижении уровня билирубина и активности печеночных трансаминаз ниже указанных предела.
Нарушение функции почек. Частота возникновения побочных реакций III и IV степени у больных с нарушением функции почек средней степени тяжести (клиренс креатинина – 30-50 мл / мин) повышенная по сравнению с общей группой пациентов.
Поскольку препарат содержит лактозу в качестве вспомогательного вещества, пациентам с врожденной непереносимостью галактозы, дефицитом лактазы Лаппа, нарушением всасывания глюкозы-галактозы не следует применять препарат.
Применение у пациентов пожилого возраста .
У больных с метастазирующим колоректальным раком в возрасте 60-79 лет, которые получали препарат в режиме монотерапии, частота возникновения желудочно-кишечного токсичности была подобной такой в группе пациентов в целом. У больных старше 80 лет явления желудочно-кишечной токсичности (диарея, тошнота и рвота) III и IV степеней развивались чаще, чем у молодых. При применении препарата в комбинации с другими лекарственными средствами у больных пожилого возраста (≥ 65 лет) отмечалась большая частота нежелательных эффектов III и IV степеней токсичности, которые привели к отмене лечения, по сравнению с больными более младшего возраста. При лечении препаратом в комбинации с доцетакселом у больных старше 60 лет отмечалось увеличение частоты нежелательных эффектов III и IV степеней токсичности, серьезных побочных явлений, связанных с лечением, и ранней отмены лечения в связи с побочными явлениями сравнению с таковыми у больных в возрасте до 60 лет.
Больные пожилого возраста с нарушениями функции почек
Больных с нарушением функции почек, которым суждено Капецитабин, необходимо тщательно наблюдать. Частота побочных явлений III и IV степени тяжести, связанных с применением 5-ФУ, была выше у больных с умеренной почечной недостаточностью (клиренс креатинина 30-50 мл / мин).
Больные пожилого возраста с нарушениями функции печени
Больных с нарушением функции печени, которым суждено Капецитабин, необходимо тщательно наблюдать. Влияние нарушения функции печени, не предопределены метастазами в печень или тяжелым нарушением функции почек, на распределение препарата неизвестен.
Применение в период беременности или кормления грудью.
Капецитабин следует считать потенциальным тератогеном для человека. Применение препарата беременным изучалось, однако, основываясь на фармакологических и токсикологических свойствах препарата, можно предположить, что применение Капецитабина может быть вредным для плода при применении беременным. В ходе исследований репродуктивной токсичности у животных капецитабин вызывал ембриолетальнисть и тератогенность, которые являются ожидаемыми эффектами производных фторпиримидина. В период беременности применять препарат не следует. Если препарат назначают в период беременности или беременность наступает у пациентки, которая уже принимает этот препарат, ее следует предупредить о возможной опасности для плода. Женщинам репродуктивного возраста необходимо рекомендовать избегать беременности во время лечения.
Неизвестно, проникает ли препарат в грудное молоко. В грудном молоке лактирующих животных были обнаружены значительные количества метаболитов капецитабина. Поэтому при лечении Капецитабином не рекомендуется младенцев кормить грудью.
Способность влиять на скорость реакции при управлении автотранспортом или работе с другими механизмами.
Препарат имеет незначительный или умеренное влияние на способность управлять транспортными средствами и работать со сложными механизмами. Капецитабин может вызвать головокружение, слабость и тошноту.
Утилизация неиспользованного препарата и препарата с истекшим сроком годности . Поступления препарата во внешнюю среду необходимо свести к минимуму. Препарат не следует выбрасывать в сточные воды и бытовые отходы. Для утилизации необходимо использовать так называемую «систему сбора отходов» при наличии таковой.
ВЗАИМОДЕЙСТВИЯ:
Антикоагулянты кумаринового ряда . Капецитабин усиливает эффекты непрямых антикоагулянтов (варфарин и фенпрокумон), что может привести к нарушению показателей свертывания и возникновения кровотечений через несколько дней или месяцев от начала терапии капецитабином, и в отдельных случаях – в течение одного месяца после окончания лечения. Во время клинического исследования после однократного введения S-варфарина в дозе 20 мг лечения приводило к увеличению AUC варфарина на 57% и MHO на 91%. Поскольку метаболизм R-варфарина не нарушался, указанное свидетельствует, что капецитабин подавляет изофермент 2С9 и не влияет на изоферменты 1А2 и ЗА4.
Больным, которые одновременно принимают капецитабин и пероральные антикоагулянты – производные кумарина, необходимо проводить детальный мониторинг показателей свертывания крови (МНО или протромбиновое время) и подбирать дозу антикоагулянта.
Субстраты цитохрома Р450 2С9 . Исследования по взаимодействию капецитабина и других препаратов, метаболизирующихся изоферментом 2С9 системы цитохрома Р450, не проводились. Необходимо с осторожностью назначать капецитабин с этими препаратами.
Фенитоин . При одновременном применении Капецитабина и фенитоина сообщалось об отдельных случаях повышение концентрации фенитоина в плазме крови, сопровождавшиеся возникновением симптомов интоксикации фенитоином. У больных, принимающих капецитабин одновременно с фенитоином, рекомендуется регулярно контролировать концентрацию фенитоина в плазме. Исследования по взаимодействию капецитабина и фенитоина не проводили, однако допускается, что в его основе лежит угнетение фермента CYP2C9 под влиянием капецитабина.
Лейковорин (фолиновая кислота). Лейковорин существенно не влияет на фармакокинетику капецитабина и его метаболитов. Однако лейковорин влияет на фармакодинамику препарата, что может привести к увеличению токсичности капецитабина, поэтому максимальная переносимая доза Капецитабина в режиме монотерапии при прерывистой схеме дозирования составляет 3000 мг / м 2 в сутки, а при комбинированном применении с лейковорином (30 мг перорально дважды в день) – только 2000 мг / м 2 в сутки.
Соривудин и его аналоги . Описаны клинически значимое взаимодействие между соривудином и 5-ФУ в результате угнетения дигидропиримидиндегидрогеназы соривудином. Такое взаимодействие потенциально может привести к летальному усиления токсичности фторпиримидинов. Поэтому Капецитабин нельзя одновременно применять с соривудином или его структурными аналогами, такими как бривудин (см. Раздел «Противопоказания»). Период между началом лечения и окончанием лечения соривудином или его структурными аналогами должен составлять не менее 4 недели.
Антациды . Влияние антацидов, содержащих алюминия и магния гидроксид, на фармакокинетику препарата изучался у пациентов с опухолями. Антациды, содержащие алюминия и магния гидроксид (Маалокс), незначительно повышают концентрации капецитабина и одного метаболита (5'-ДФЦР) в плазме; на три основных метаболита (5'-ДФУР, 5-ФУ и ФБА) капецитабина они не влияют.
Аллопуринол . Наблюдалась взаимодействие между аллопуринолом и 5-фторурацилом с возможным снижением эффективности 5-фторурацила. В связи с этим следует избегать одновременного применения Капецитабина и аллопуринола.
Интерферон альфа. Максимальная переносимая доза составляет 2000 мг / м 2 в сутки при комбинированном применении с интерфероном альфа-2а (3 млн МЕ / м 2 в сутки) по сравнению с 3000 мг / м 2 в сутки при применении препарата в режиме монотерапии.
Лучевая терапия. Максимальная переносимая доза препарата в режиме монотерапии при прерывистой схеме дозирования составляет 3000 мг / м 2 в сутки, при комбинированном применении с лучевой терапией рака прямой кишки – 2000 мг / м 2 в сутки при непрерывном курсе лучевой терапии или ежедневном 6-недельном курсе лучевой терапии в период с понедельника по пятницу.
Оксалиплатин . При комбинированном применении капецитабина и оксалиплатина с или без бевацизумаба не отмечено клинически значимой разницы в экспозиции капецитабина или его метаболитов, свободной платины и суммарной платины.
Бевацизумаб . Не отмечено клинически значимого действия бевацизумаба на фармакокинетические параметры капецитабина и его метаболитов.
Взаимодействие лекарственное средство – еда . В ходе клинических исследований пациенты были проинструктированы о приеме Капецитабина в течение 30 мин после еды. Поскольку имеющиеся данные по безопасности и эффективности базируются на применении с пищей, рекомендуется принимать Капецитабин с пищей. Прием препарата с пищей приводит к замедлению скорости всасывания капецитабина.
ПЕРЕДОЗИРОВКА:
Симптомы острой передозировки: тошнота, рвота, диарея, мукозит, раздражение желудочно-кишечного тракта и кровотечения, а также угнетение костного мозга. Лечение симптоматическое.
УСЛОВИЯ ХРАНЕНИЯ:
Хранить в оригинальной упаковке при температуре 25 ° С в недоступном для детей месте.
Общая информация
-
Форма продажи:
по рецепту
-
Действующее в-о:
Капецитабин
-
Производитель:
Гетеро Драгс Лимитед, Индия
-
Фарм. группа:
Антиметаболиты
Код ATX
-
L
Противоопухолевые препараты и иммуномодуляторы
-
L01
Противоопухолевые препараты
-
-
L01BC
Пиримидиновые аналоги
-